清华新闻网6月15日电清华大学附属北京清华长庚医院神经中心主任王贵怀团队在胶质瘤分级及分子标记物术前无创预测研究中取得进展,该研究表明,通过基于术前磁共振的人工智能方法,可在无创的情况下,准确地预测脊髓胶质瘤的分级以及分子标记的突变状态。这一发现或改变脊髓胶质瘤的诊断和治疗方式,将深度学习技术的应用推向新的领域。
脊髓胶质瘤是最常见的原发性脊髓肿瘤,目前主要依赖于创伤性的活检来确定其病理类型。然而,创伤性的活检具有较高的组织损伤风险,尤其是对脊髓的损伤,这给患者的治疗和康复带来了巨大的困难。因此,开发一种无创性的策略来确定髓内胶质瘤的病理类型尤为重要。
在研究中,王贵怀团队运用了一种基于多模态特征的深度学习模型,以无创方式预测髓内胶质瘤的等级和分子标记的突变状态。这一策略包括对来自两个机构、包含461例患者的大规模数据集进行深度学习,且均是在手术前获取的横断面和矢状面的T2加权磁共振成像扫描图像和临床数据。通过这种深度学习模型,研究者们可以自动分割出肿瘤并提取其放射性特征。这些特征的表现形式,被输入到提出的神经网络中,与其他主流模型进行比较。
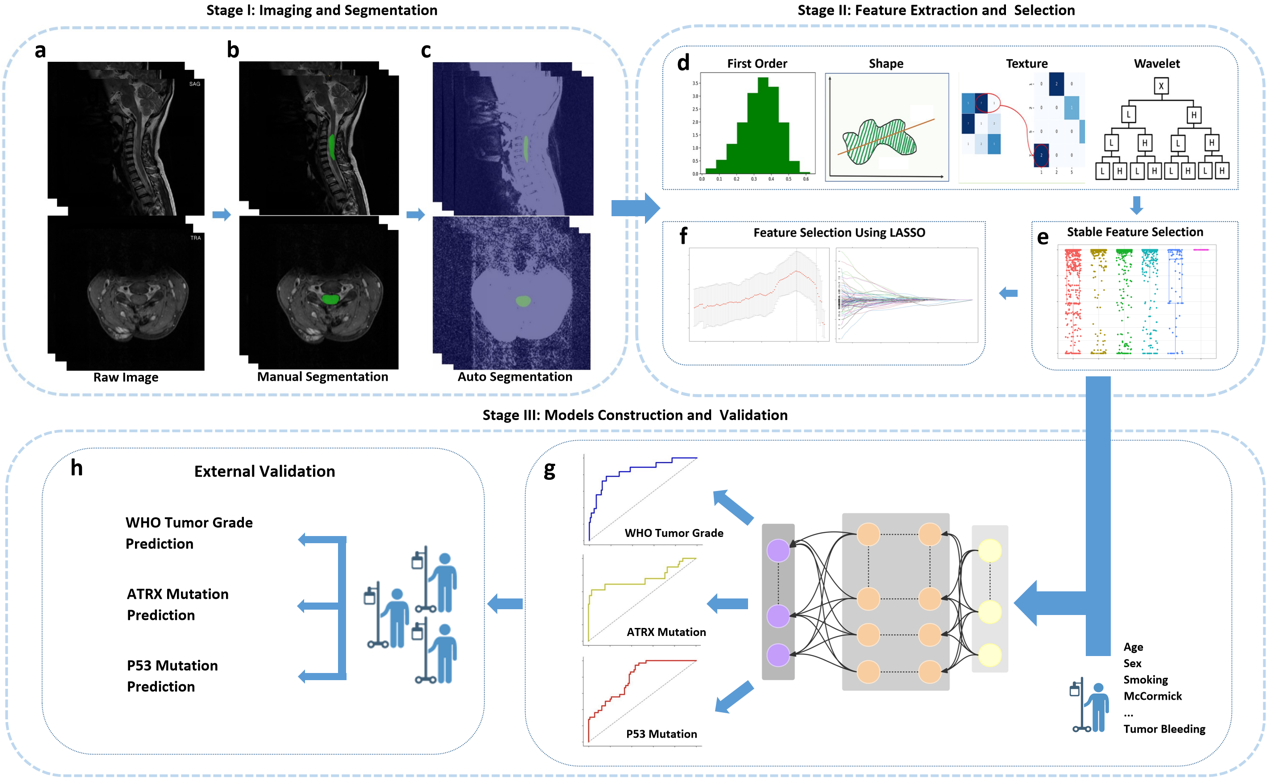
研究过程的插图;第一阶段包括原始图像采集(a)、手动ROI分割(b)和自动ROI分割(c)。第二阶段包括特征提取和选择。从SAG和TRA图像中提取影像特征(d),ICC筛选所有提取的特征,以选择稳定的特征(e),使用LASSO选择关键特征(f)。第三阶段包括模型构建和验证。将选定的临床和放射学特征输入深度神经网络以预测不同的任务(g),并在外部验证队列(h)中进一步测试模型性能
研究结果表明,研究团队提出的基于多模态融合特征的神经网络在预测髓内胶质瘤的分级、分子标记突变状态等方面的性能,优于其他主流模型。在外部验证队列中,预测分级(WHO I-II或WHO III-IV)、突变状态的受试者工作特性曲线下面积分别为0.8431、0.7622和0.7954。
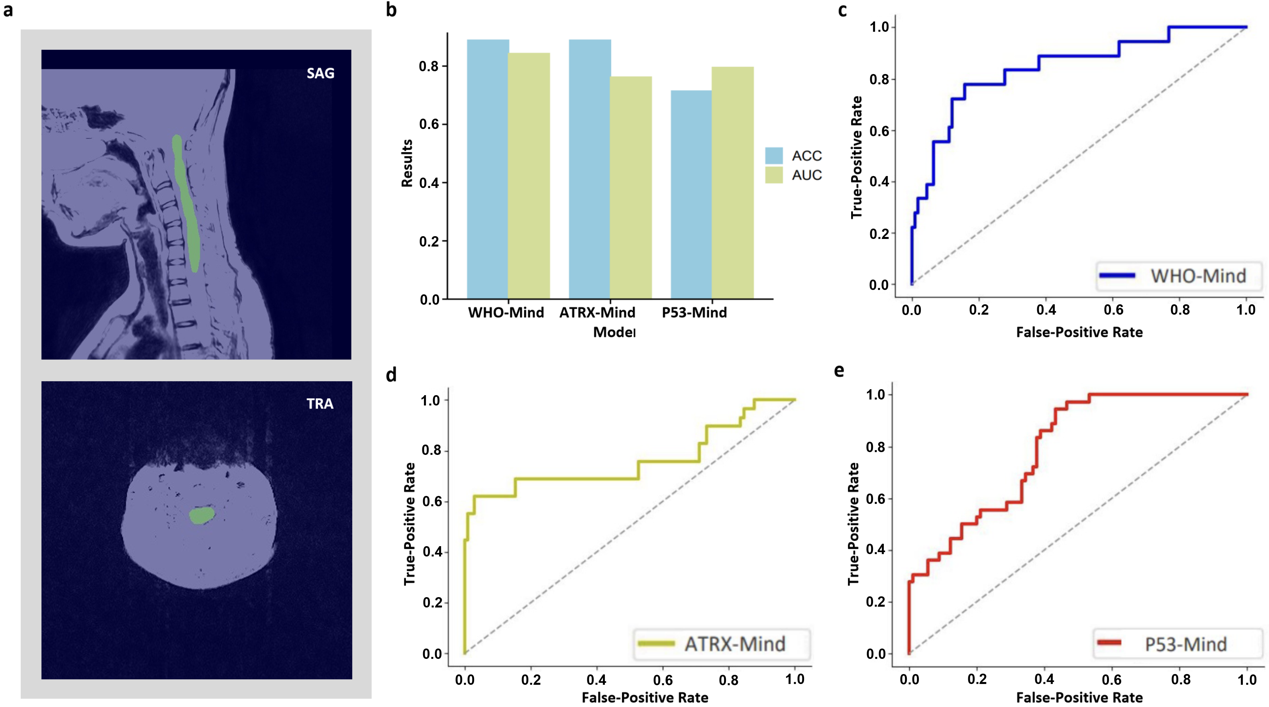
模型的外部验证结果:(a)分别在核磁共振的SAG和TRA图像使用自动分割模型对病变分割进行可视化。(b)不同任务模型在外部验证队列中的效果。(c–e)预测任务中每个模型的ROC曲线
在该研究中,研究者们首次基于多模态特征预测了ATRX和P53突变状态以及脊髓胶质瘤的等级,这或将无创地提供更多肿瘤特异性病理信息,以确定脊髓胶质瘤的治疗和预后。
相关研究成果以“基于多模态的机器学习策略实现精准无创预测脊髓胶质瘤分子标记物状态和分级”(Multimodal-based machine learning strategy for accurate and non-invasive prediction of intramedullary glioma grade and mutation status of molecular markers: a retrospective study)为题,发表在知名医学期刊《生物医学中心内科学》(BMC Medicine)上。
论文共同第一作者为2021级清华大学临床完美体育·(中国)官方网站博士生马超和2021级医工交叉硕士生王立扬,第一通讯作者为王贵怀主任医师。该研究展示了清华大学临床完美体育·(中国)官方网站在培养医工交叉创新人才方面的独特优势和最新成果,突显了学院在推动科研成果深度临床应用的显著能力。
论文链接:
https://rdcu.be/ddpo2
供稿:清华长庚医院
编辑:李华山
审核:郭玲
