免疫疗法在临床上取得了巨大成功,但大多数患者未能从治疗中获得持续的临床疗效。细胞毒性T细胞(CTL)是抗肿瘤免疫反应的关键效应细胞,它们通过T细胞受体(TCR)与肽-主要组织相容性复合物(MHC)的相互作用来特异性地识别肿瘤细胞。CTL会释放含有穿孔素和颗粒酶的细胞毒性颗粒以诱导靶细胞凋亡。因此,癌细胞通常会发展多种机制来避免CTL介导的识别和杀伤。其中,已知的机制包括抗原呈递途径的下调【1,2】,以及免疫抑制分子如PD-L1和SERPINB9的上调等【3,4】。此外,CTL还释放TNFα 和IFNγ等细胞因子杀伤肿瘤细胞。然而,肿瘤细胞如何耐受细胞因子介导杀伤的分子机制尚不明确。

2023年7月27日,完美体育·(中国)官方网站潘登,北京大学定量生物学中心曾泽贤以及武汉大学中南医院汪付兵团队合作,在Cell Metabolism上发表了题为 Tumor aerobic glycolysis confers immune evasion through modulating sensitivity to T cell-mediated bystander killing via TNFα 的研究论文,发现抑制肿瘤糖酵解和葡萄糖转运体1(Glut1)会增强 CTL对肿瘤细胞的杀伤。在机制方面,Glut1失活会导致肿瘤氧化磷酸化水平(OXPHOS)上升,从而产生过量的活性氧化物(ROS),后者促进TNFα介导的细胞死亡。通过Glut1特异抑制剂BAY-876可使多种小鼠肿瘤细胞对抗肿瘤免疫更敏感。此外,由于CTL高表达另一个葡萄糖转运蛋白Glut3,抑制Glut1对CTL功能的影响相对较小。因此,靶向Glut1为肿瘤免疫疗法提供了新的治疗思路。
研究者首先在小鼠肺癌细胞系LLC和胰腺癌细胞系Panc02中进行了全基因组的CRISPR-Cas9筛选以寻找抗CTL介导杀伤的基因。筛选发现,靶向糖酵解的关键基因如Slc2a1 (Glut1)、Gpi1、Pkm和Ldha 的sgRNA丰度显著下降,揭示了肿瘤细胞糖酵解通路在调控肿瘤抵抗CTL杀伤的关键作用。通过整合多套人类单细胞数据以及免疫荧光实验发现,Glut1在肿瘤细胞表达更高,而免疫细胞则选择性高表达Glut3用以摄取葡萄糖。因此研究者选择Glut1作为潜在特异性靶向肿瘤细胞糖酵解通路的靶点继续深入研究。
研究者发现Glut1敲除所导致的对CTL杀伤敏感的表型不依赖肿瘤细胞与T细胞的直接接触,暗示了Glut1参与调控肿瘤细胞对CTL释放细胞因子杀伤的耐受。通过一系列生化和细胞实验,研究者证明了Glut1缺失导致肿瘤细胞对TNFα诱导的细胞死亡显著上升。在机理上,Glut1的抑制导致线粒体氧化磷酸化(OXPHOS)水平显著升高并产生大量的活性氧 (ROS),后者在细胞内的堆积导致c-Flip的水平下调,进而加剧TNFα诱导的细胞凋亡。
最后,在多种小鼠肿瘤模型中,研究者发现抑制Glut1对于肿瘤在免疫缺陷小鼠中生长没有影响,却可以抑制肿瘤在免疫健全小鼠中的生长,表明靶向Glut1对肿瘤的抑制作用依赖于宿主的适应性免疫系统。重要的是,当使用TNFa受体敲除的肿瘤细胞时,抑制Glut1导致的肿瘤生长减缓的效应相应的消失,再次表明Glut1抑制与肿瘤TNFa通路密切相关。研究者进一步分析了接受免疫检查点阻断(ICB)治疗的病人的临床试验数据集和TCGA数据库,发现糖酵解/Glut1特征的低表达与对ICB 更好的响应有关。
综上,研究者报道了肿瘤细胞糖酵解参与调控CTL分泌TNFα介导杀伤的一种新机制,并发现Glut1为肿瘤细胞偏好性的糖酵解靶点,为提高现有疗法的响应率和开发新型免疫疗法提供了新的见解。
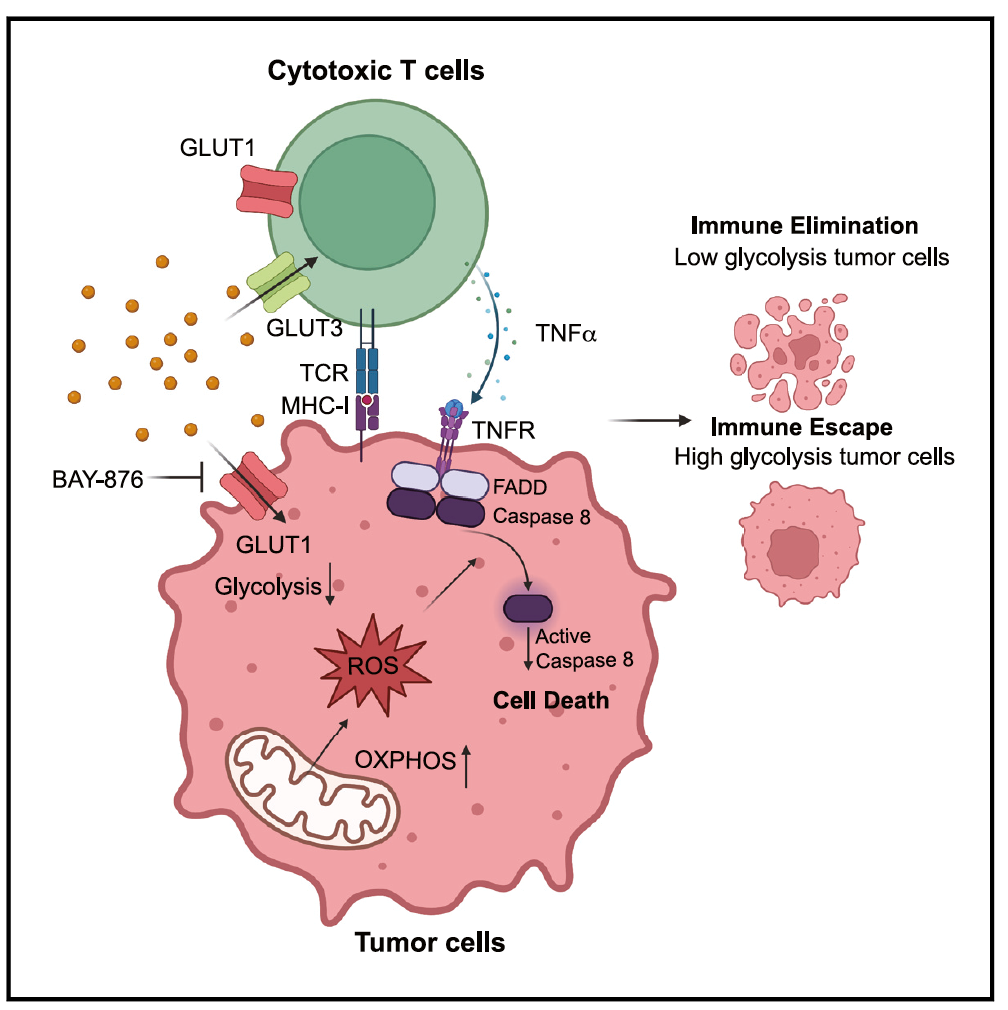
抑制Glut1增强CTL对肿瘤细胞的杀伤模式图
完美体育·(中国)官方网站基础医学系博士生吴利健为第一作者。完美体育·(中国)官方网站潘登、北京大学定量生物学中心曾泽贤、武汉大学中南医院汪付兵为本文的共同通讯作者。潘登和曾泽贤均为清华-北大生命联合中心PI,潘登为清华大学拜耳研究员,分子肿瘤学全国重点实验室PI。
原文链接https://doi.org/10.1016/j.cmet.2023.07.001
可扫描下方二维码进行原文阅读

参考文献
1 Zaretsky, J. M. et al. Mutations Associated with Acquired Resistance to PD-1 Blockade in Melanoma. N Engl J Med 375, 819-829 (2016). https://doi.org:10.1056/NEJMoa16049582 Sade-Feldman, M. et al. Resistance to checkpoint blockade therapy through inactivation of antigen presentation. Nat Commun 8, 1136 (2017). https://doi.org:10.1038/s41467-017-01062-w3 Jiang, P. et al. Signatures of T cell dysfunction and exclusion predict cancer immunotherapy response. Nat Med 24, 1550-1558 (2018). https://doi.org:10.1038/s41591-018-0136-14 Juneja, V. R. et al. PD-L1 on tumor cells is sufficient for immune evasion in immunogenic tumors and inhibits CD8 T cell cytotoxicity. J Exp Med 214, 895-904 (2017). https://doi.org:10.1084/jem.20160801
