清华大学药学院王钊教授课题组以“Effects of Maillard reaction and its product AGEs on aging and age-related diseases”为题在食品科技领域专业期刊Food Science and Human Wellness杂志在线发表综述文章,以晚期糖基化终末产物(Advanced glycation end products,AGEs)为主要讨论对象,希望人们重视美拉德反应(Maillard reaction,MR)与人类衰老和健康之间的潜在联系,合理控制饮食和规划生活方式。
1、什么是美拉德反应
美拉德反应,得名源于法国早期研究蛋白质生物合成的生物化学家Louis-Camille Maillard,(1878-1936)偶然发现了氨基酸和糖的混合物在加热时会发生不同程度的褐变。理论的发展总是在不断补充中曲折完善的,目前已经明确定义MR是羰基化合物(主要是还原糖)与氨基酸、胺或蛋白质等含有游离氨基的物质之间的非酶褐变反应。
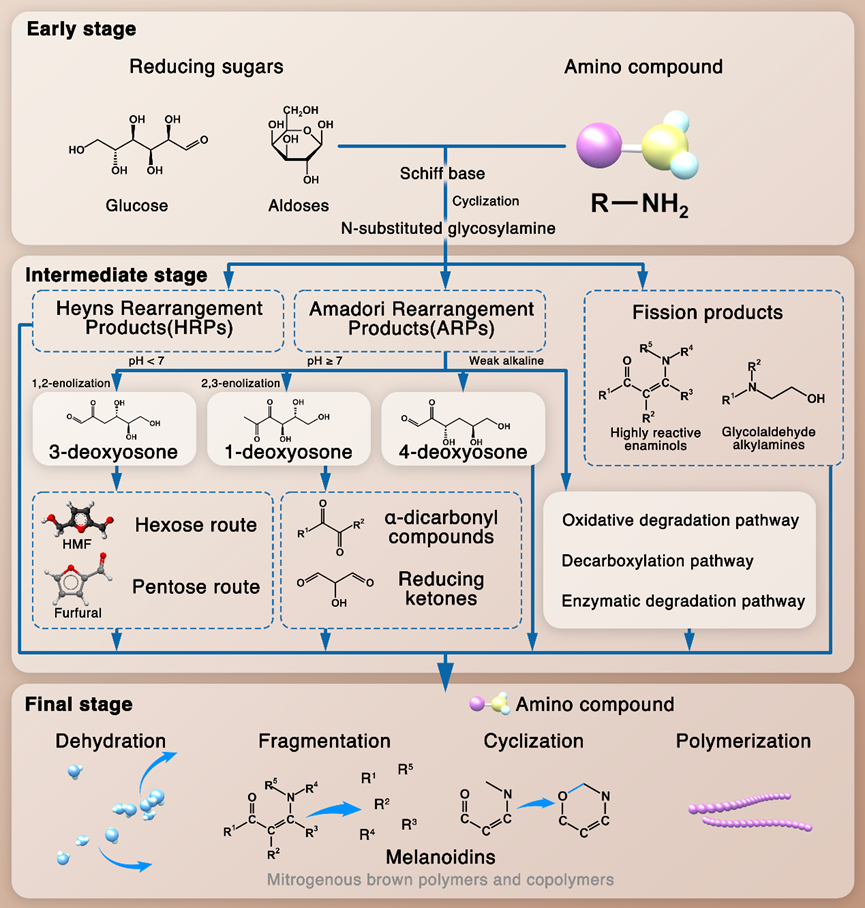
图1 美拉德反应的三个阶段示意图
2、AGEs的积累和代谢
到目前为止,与年龄相关的美拉德反应产物(Maillard reaction products,MRPs)研究多集中在AGEs上,某些AGEs的水平已被作为衰老或相关疾病的生物标志物。AGEs存在于人体的血液和组织中,加上饮食中发现的AGEs,已鉴定的AGEs有20多种,可分为荧光型和非荧光型(图2)。在高温下烹饪获得的高蛋白或脂肪含量的食物富含膳食AGEs。据统计,我们平均每天在饮食中摄入约75 mg AGEs,其中约30% - 80%被消化系统吸收,但这一关于人体吸收的统计数据仍存在争议。此外,组织内AGEs的蓄积受多种因素调节,包括靶蛋白的周转率、代谢率、氧化还原平衡、糖水平、解毒系统活性等,主要影响长寿蛋白的功能,如胶原蛋白、层粘连蛋白、弹性蛋白、血红蛋白、溶菌酶和碱性磷酸酶。糖基化引起的蛋白质构象改变可以抵抗蛋白质降解,促进无法发挥正常生理功能的蛋白质在细胞和器官内的积累。
在生物有机体中,衰老过程具有普遍性、进行性、不可逆性和危害性。大量研究发现,MR在导致体内营养物质损失和有毒有害化合物产生的同时,通过几种有害过程促进与衰老相关的组织结构和功能的年龄依赖性衰退。内源性形成的AGEs可能积聚在细胞内和细胞外的蛋白质、脂质和核酸上,并与氧化应激、高血糖和高脂血症等病理变化以及各种炎症有关。
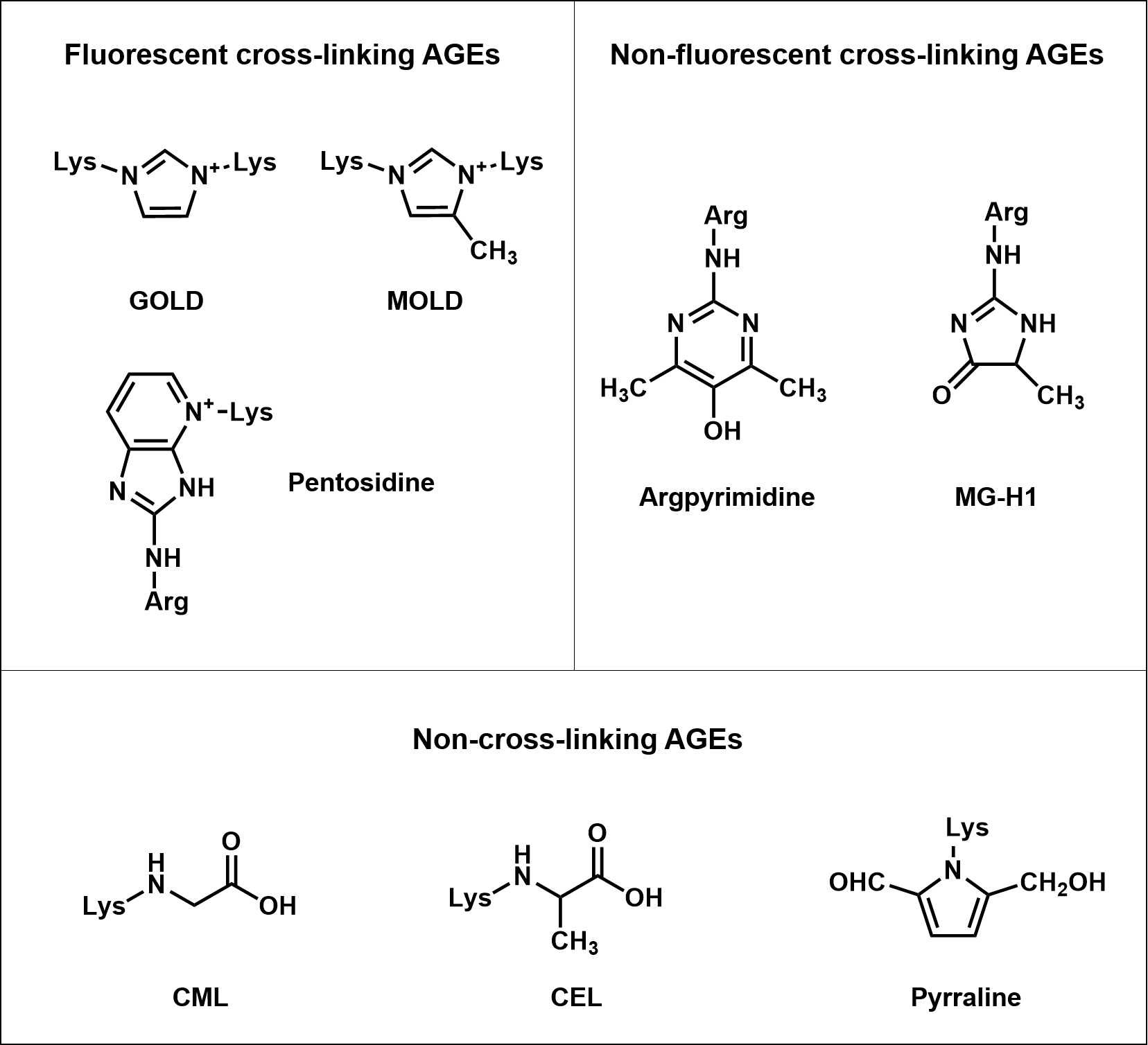
图2 具有代表性AGEs的结构
3、对生理性衰老的影响
具有长寿命蛋白质的组织,如晶状体、动脉、肌腱、肺、软骨或皮肤,通常会随着年龄的增长而失去弹性或硬度增加。这种现象不仅是由弹性蛋白或胶原蛋白含量的变化引起的,一方面,MRPs含量与年龄相关的僵硬、蛋白质消化率和组织弹性损失相关。随着年龄的增长,还原糖和蛋白质一级氨基之间的非酶促MR形成的AGEs会增加组织蛋白质的化学修饰和交联,慢性修饰损害蛋白质水解消化率并改变蛋白质构象。另一方面,AGEs在组织中的积累也刺激了过度的氧化应激和细胞因子的释放,从而影响胞外基质(Extracellular matrix,ECM)的更新。

图3 MRPs对生理性和病理性衰老的影响
4、对病理性衰老的影响
综述主要关注AGEs与自身免疫和炎症性疾病、神经退行性疾病、糖尿病和糖尿病肾病、心血管疾病和骨退行性疾病的关联性。一方面,这些疾病都与炎症信号有着密切的关系,而AGE受体(Receptor of AGE,RAGE)在慢性炎症和免疫功能障碍中起着不可忽视的作用。RAGE作为一种多配体跨膜受体,除了与AGEs结合外,还可以与其他配体结合,包括the DNA binding protein high-mobility group box-1 (HMGB-1)/amphoterin,S100 calgranulins,Mac-1和Aβ肽(Amyloid-β peptide,Aβ)。在释放这些配体分子后,RAGE可能激活自分泌和旁分泌信号通路,从而放大组织炎症和损伤。AGE-RAGE的相互作用,涉及四个转导信号通路,分别是JAK2- signal transducer and activator of transcription 1 (STAT1),PI3K-AKT,MAPK-ERK和NADPH oxidase-ROS。通过这些途径,磷酸化的NF-κB最终进入细胞核转录促炎因子、生长因子、促纤维化因子和氧化应激的基因表达。另一方面,Aβ、tau蛋白、α-突触核蛋白、朊病毒等蛋白积累,可以被AGEs修饰而糖基化,促进异常聚集,引发病理性损伤的增强和细胞凋亡。AGEs与胶原蛋白、弹性蛋白和其他大分子上的氨基发生反应,弹性纤维的断裂和胶原纤维的交联导致大分子结构刚性增加和血管壁逐渐硬化。AGEs对骨生物力学性能的有害影响部分是由于细胞外环境中长期存在的基质蛋白(如胶原I,约占骨总胶原含量的95%),长期暴露于AGEs的骨蛋白不可逆交联导致其抵抗降解,结构和功能发生变化,影响成骨细胞的增殖和分化。
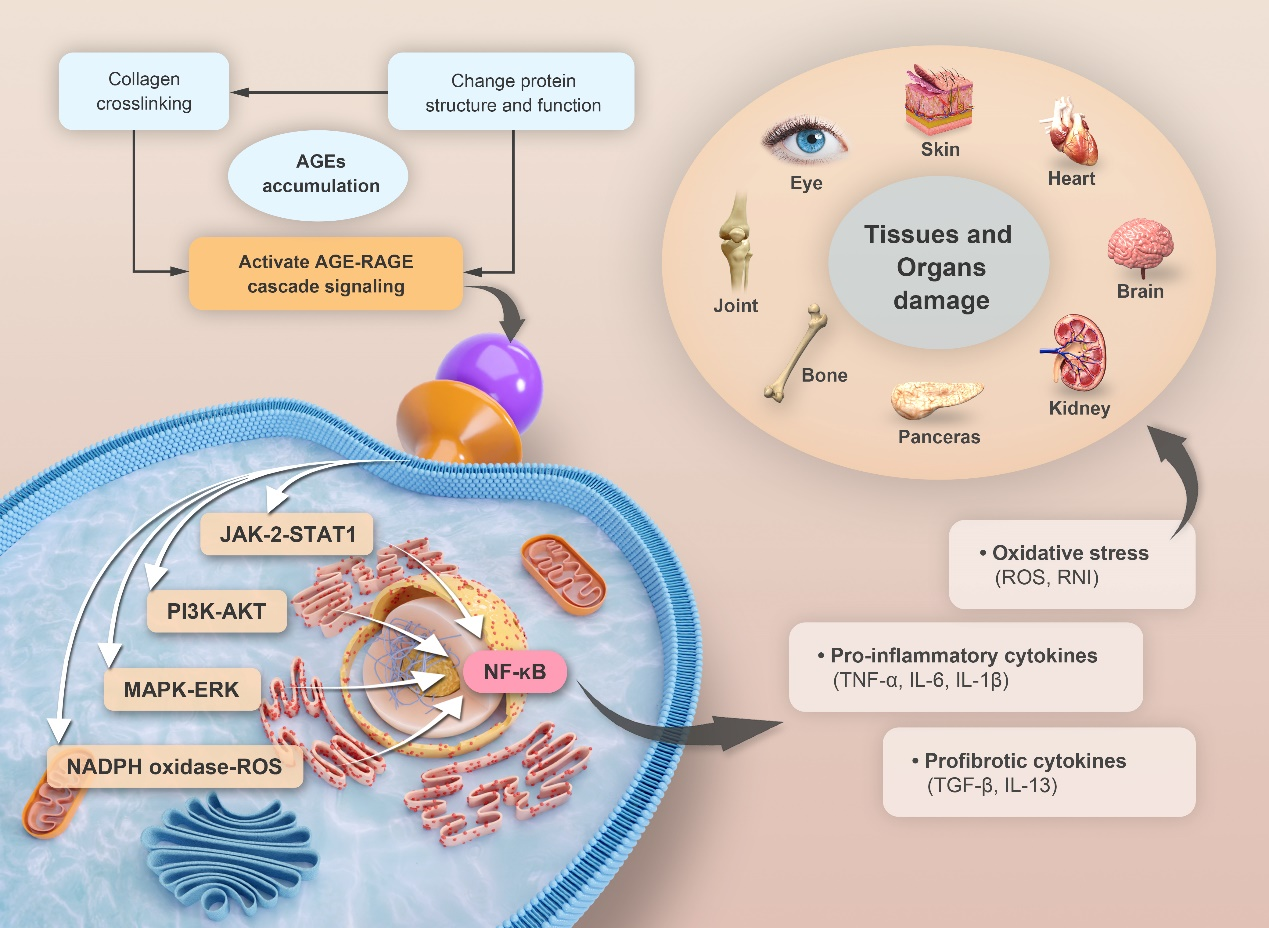
图4 AGEs加速衰老及相关疾病的机制
5、MR的干预和控制
机体中过量有害的MRPs在一定程度上加速了衰老过程和增龄相关疾病的发生,使机体受到潜移默化的侵害。因此,目前出现的有效干预措施包括药物干预,主要通过糖基化的衰减、氧化应激的抵抗、金属离子的螯合、活性1,2-二羰基化合物或ROS/RNI的去除来减缓或消除AGEs对疾病的不利影响,但是很多药物在临床前研究和临床试验中被发现具有潜在毒性和副作用,仍然没有FDA批准的药物可用于治疗诱导的病理症状。
我们需要重视的是饮食和生活习惯的养成,事实上,膳食AGEs是机体AGEs池中最重要的外源AGEs来源之一,限制富含AGEs的饮食有利于降低可引起氧化应激和炎症的有效总AGEs水平,我们应注意合理控制高碳水饮食、高热量饮食、高温加工食品的日常习惯。同时,个人吸烟习惯会加速AGEs的产生和外源积累,并有可能发展为慢性阻塞性肺疾病和皮肤老化。不仅如此,吸烟引发的AGEs的积累还会通过母乳转移。此外,久坐不动的生活方式也会造成AGEs的形成,这就要求我们保持良好的生活习惯,对自己和亲人的健康负责。
多吃蒸、煮、炖,少吃煎、烤、炸。健康生活每一天!
清华大学药学院王钊教授为本文通讯作者,药学院2022级博士生彭欢为文章第一作者。课题组成员高钰琪、曾晨叶、花瑞、郭彦南、王译达为本工作提供了重要帮助。本工作得到了国家自然科学基金、清华大学春风基金的支持。
原文链接:https://www.sciopen.com/article/10.26599/FSHW.2022.9250094
