近日,清华大学药学院杨悦课题组在国际知名的柳叶刀子刊《The Lancet Regional Health-Western Pacific》在线发表了题为《我国国产和进口同类抗肿瘤靶向药的评估:价格、有效性和安全性方面的比较研究》(The Price, Efficacy, and Safety of Within-Class Targeted Anticancer Medicines between Domestic and Imported Drugs in China: A Comparative Analysis)的研究长文。

研究概述
根据世界卫生组织2020年数据显示,我国新确诊的癌症患者近457万例,死亡病例高达300万人,其癌症发病率和死亡率已位居世界首位。每年所需的肿瘤医疗费用超过2200亿元,过去五年里中国的抗癌药物支出增加超过一倍,抗肿瘤药物的可负担性已经成为目前我国公共卫生领域所面临的主要问题。自2015年以来,我国启动一系列改革措施,包括药品审评审批改革和国家医保药品目录准入,旨在提高我国抗肿瘤药物的可负担性,惠及更多患者 (图-1)。根据国家药品监督管理局药品审评中心发布的年度药品报告,由我国本土制药企业研发的抗肿瘤靶向药在数量和品种方面均取得了突破性进展。同时,由国家医疗保障局开展的多轮国家药品价格谈判,抗肿瘤靶向药价格平均降低幅度超过了50%,这对改善患者用药可负担性具有重要的意义。然而,关于国产和进口同类抗肿瘤靶向药(同类抗肿瘤靶向药定义为具有相同靶点用于治疗相同适应症的抗肿瘤药品)在月治疗费用是否存在差异方面的证据非常有限。更为关键的是国产同类抗肿瘤药与进口相比,是否能够为患者提供足够的有效性和安全性尚不清楚。
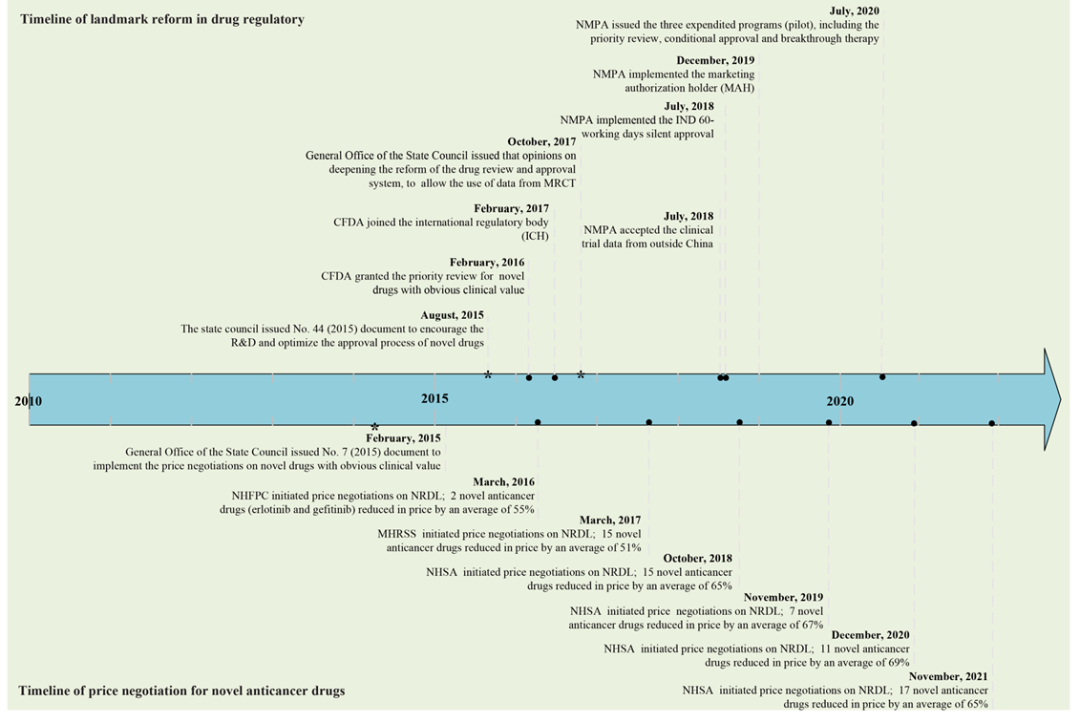
图-1 我国药品审批审评改革和国家医保谈判发展历程
为解决上述问题,课题组系统评估我国国产和进口同类抗肿瘤靶向药的价格(首发上市和最新的月治疗费用)、有效性和安全性。该研究纳入了2010 -2022年获批上市的12组同靶点同适应症的国产和进口抗肿瘤靶向药(每组至少1个国产和进口抗肿瘤靶向药)。研究结果显示国产和进口同类抗肿瘤靶向药自上市以来月治疗费用分别降低了71%和62%,这主要由于国家医保药品价格谈判的重要作用。与进口抗肿瘤靶向药相比,国产同类抗肿瘤靶向药的首发上市和最新的月治疗费用中位数均显著低于进口抗肿瘤。同时,国产和进口同类抗肿瘤靶向药在有效性和安全性方面并无显著差异。这些证据支持了近年来药品审批审评改革(国产同类抗肿瘤靶向药的上市)和国家医保谈判对于改善我国肿瘤患者用药可负担性发挥了不可替代的重要作用,同时为解决全球肿瘤患者用药可负担性问题提供了中国方案。此次研究也为更多国产同类抗肿瘤靶向药走向全球提供了强有力的证据。
(一)国产抗肿瘤靶向药比进口同类药更具价格优势
相比于首发上市时的月治疗费用,最新(2022年)的国产和进口抗肿瘤靶向药月治疗费用均呈明显降价趋势 (图-2)。国产和进口药物的月治疗费用中位数分别下降了71% (P<0.001)和62% (P<0.001)。此外,国产抗肿瘤靶向药的首发上市 (3786$ vs. 5393$,P=0.007)和最新 (1222$ vs. 2077$, P=0.01)的月治疗费用中位数均显著低于同类进口抗肿瘤药物 (图-3)。以PD1/PDL1靶向药用于治疗非小细胞肺癌为例,国产PD1/PDL1靶向药月治疗费用中位数仅为878$,远远低于进口同类抗肿瘤靶向药(7667$), 这也使中国患者有望享受全球最低的PD1/PDL1靶向药治疗价格。
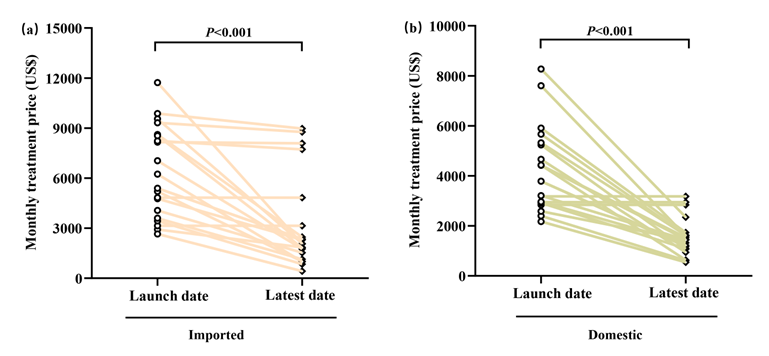
图-2 对比进口和国产同类抗肿瘤靶向药在首发上市和最新(2022年)月治疗费用变化
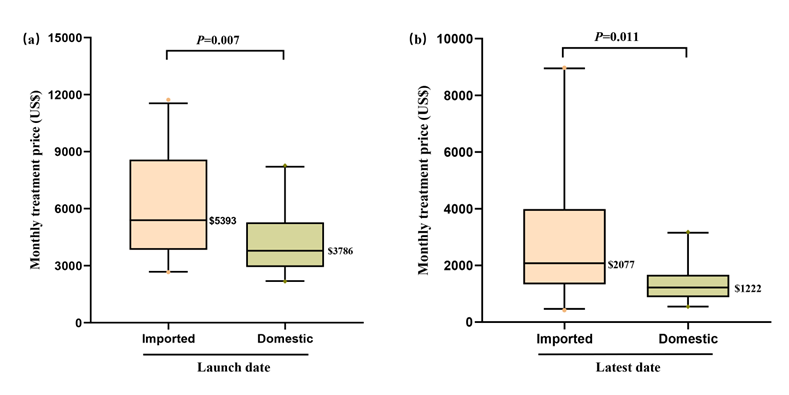
图-3对比进口和国产同类抗肿瘤靶向药在首发上市和最新(2022年)月治疗费用的差异
(二)国产和进口同类抗肿瘤靶向药在有效性方面无显著差异
在证明国产抗肿瘤靶向药比进口同类药更具价格优势后,课题组对国产和进口抗肿瘤靶向药主要有效性指标进行评估,包括总生存期(OS)、疾病无进展生存期(PFS)和客观缓解率(ORR)。结果显示,国产和进口抗肿瘤靶向药的OS指标无显著差异(HR: 0.71 vs. 0.66, P=0.38)(图-4);PFS指标无显著差异(HR: 0.51 vs. 0.48, P=0.60)(图-5);ORR中位数也无显著差异(ORR: 37% vs. 48%;P=0.51)(图-6)。
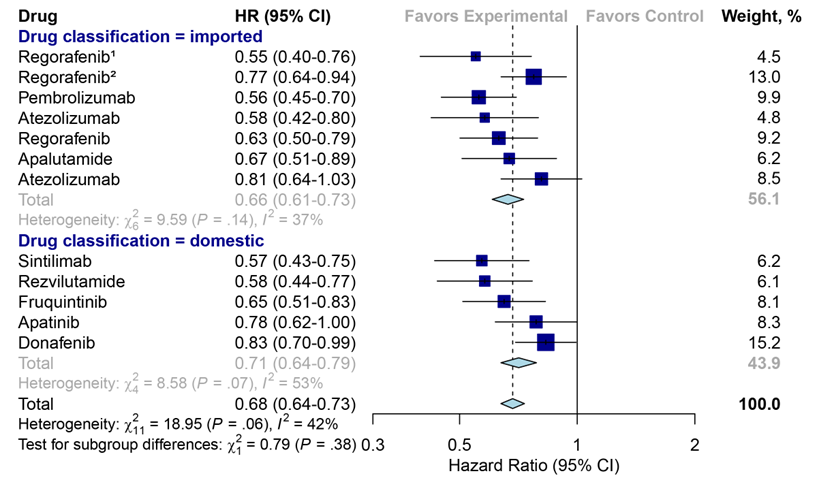
图-4 对比国产和进口同类抗肿瘤靶向药总生存期(OS)差异
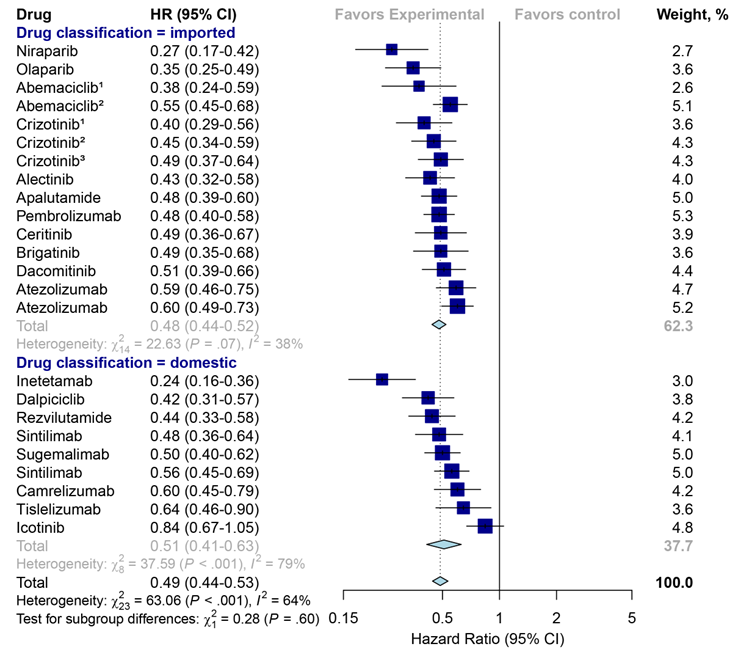
图-5 对比国产和进口同类抗肿瘤靶向药的疾病无进展生存期(PFS)的差异
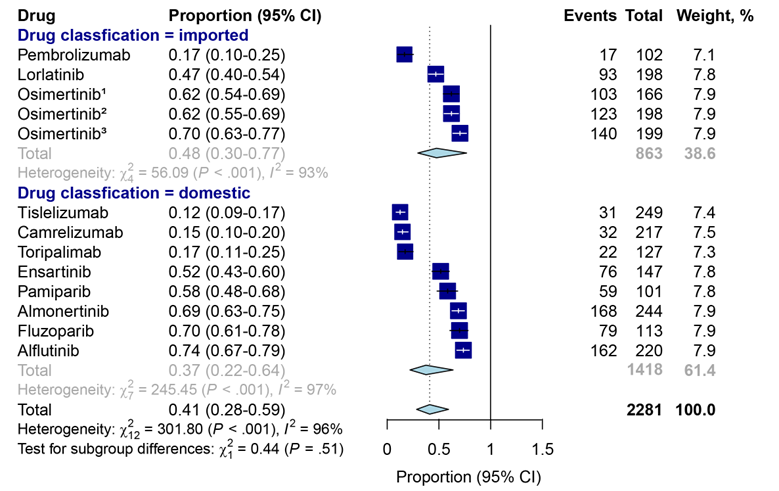
图-6 对比国产和进口同类抗肿瘤靶向药的客观缓解率(ORR)的差异
(三)国产和进口抗肿瘤靶向药在安全性上无显著差异
在证明国产抗肿瘤靶向药和进口同类药在有效性方面并无显著差异后,课题组进一步对国产和进口抗肿瘤靶向药的安全指标进行评估,包括严重不良反应(SAE)发生率和GRADE≥3级不良事件(GRADE ≥3 AEs)发生率。结果显示,国产和进口抗肿瘤靶向药在SAE发生率(RR: 1.40 vs 1.18,P=0.23)(图-7)和GRADE≥3级不良事件(RR: 1.57 vs 1.61,P=0.92)方面均无显著差异 (图-8)。
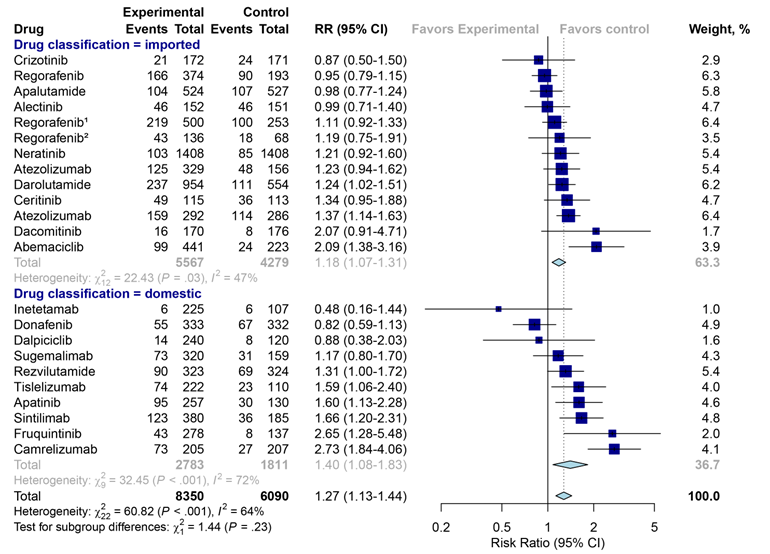
图-7 对比国产和进口同类抗肿瘤靶向药的严重不良反应(SAE)差异
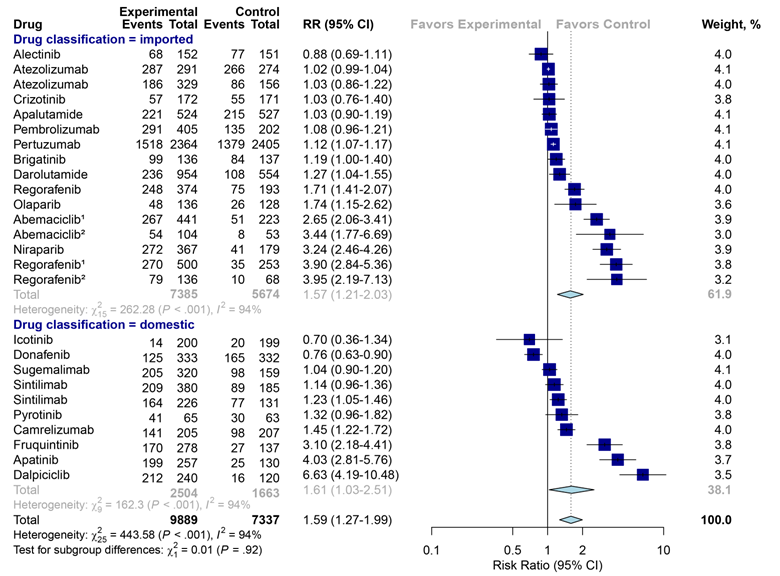
图-8 对比国产和进口同类抗肿瘤靶向药的GRADE≥3级的不良反应差异
总 结
综上所述,我国国产同类抗肿瘤靶向药不仅在价格方面显著优于进口,在有效性和安全性方面同样达到了相当水平。该研究支持我国应当进一步鼓励创新药的研发,将更多的抗肿瘤靶向药纳入国家医保目录谈判,让肿瘤靶向药惠及更多中国和全球的患者。
参考文献
[1] Luo X, Yang L, Du X, Yang J, Qian F, Yang Y. Analysis of Patent and Regulatory Exclusivity for Novel Agents in China and the United States: A Cohort Study of Drugs Approved Between 2018 and 2021. Clin Pharmacol Ther. 2022 Aug;112(2):335-343.
[2] Vokinger KN, Hwang TJ, Carl DL, et al. Price changes and within-class competition of cancer drugs in the USA and Europe: a comparative analysis. The Lancet Oncology 2022; 23(4): 514-20.
[3] Hwang TJ, Franklin JM, Chen CT, et al. Efficacy, Safety, and Regulatory Approval of Food and Drug Administration-Designated Breakthrough and Nonbreakthrough Cancer Medicines. J Clin Oncol 2018; 36(18): 1805-12.
致 谢
本文通讯作者为清华大学药学院杨悦研究员和杜克大学完美体育·(中国)官方网站周贤忠教授,第一作者为清华大学药学院博士后罗兴献和青年学者杜鑫。北京大学人民医院黄琳主任、薛学财和周越博士,复旦大学药学院谭睿洁(2022年清华大学药学院安进学者),清华大学药学院科研助理过其祥和李壮琪以及中国医学科学院肿瘤医院乐凯迪和李泰锋博士对该研究提供了大力支持和协助。感谢药学院钱锋院长课题组对该研究提供的帮助和支持。该项研究得到了清华-北京大学生命科学联合中心基金的项目经费支持。
